辦理條件
1、產品研制、生產工藝文件規定的要求
2、有保證醫療器械質量的管理制度
3、有與生產的醫療器械相適應的生產場地、環境條件、生產設備以及專業技術人員
4、有對生產的醫療器械進行質量檢驗的機構或者專職檢驗人員以及檢驗設備
5、有與生產的醫療器械相適應的售后服務能力
申請材料清單
1、產品技術要求
2、《第一類醫療器械備案表》
3、產品說明書及最小銷售單元標簽設計樣稿
4、符合性聲明
5、臨床評價資料
6、風險分析報告
7、產品檢驗報告
8、授權委托書
9、生產制造信息
10、證明性文件
辦理流程
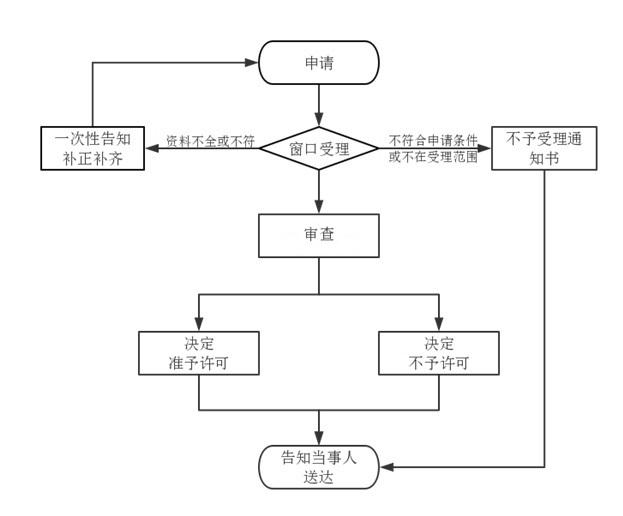
凱納德相關服務
●產品技術要求審核
●產品臨床評價資料審核
●產品標簽,說明書,包裝文件審核
●產品檢測要求確定
●產品備案資料編寫與定稿
●產品技術要求確認
●產品備案資料遞交
廣東凱納德企業管理咨詢有限公司
聯系人:汪先生
熱線:0757-83836955
QQ:530756778
地址:廣東省佛山市南海區桂城季華東路31號天安中心7座303A
專業ISO9001認證、ISO14001認證、ISO45001認證、IATF16949認證等體系認證咨詢機構
Copyright ? 廣東凱納德企業管理咨詢有限公司 版權所有 粵ICP備19080410號-2